Қазақстандықтарға салынып жатқан "Спутник V" вакцинасының нұсқаулығында не жазылған
Опубликовано:
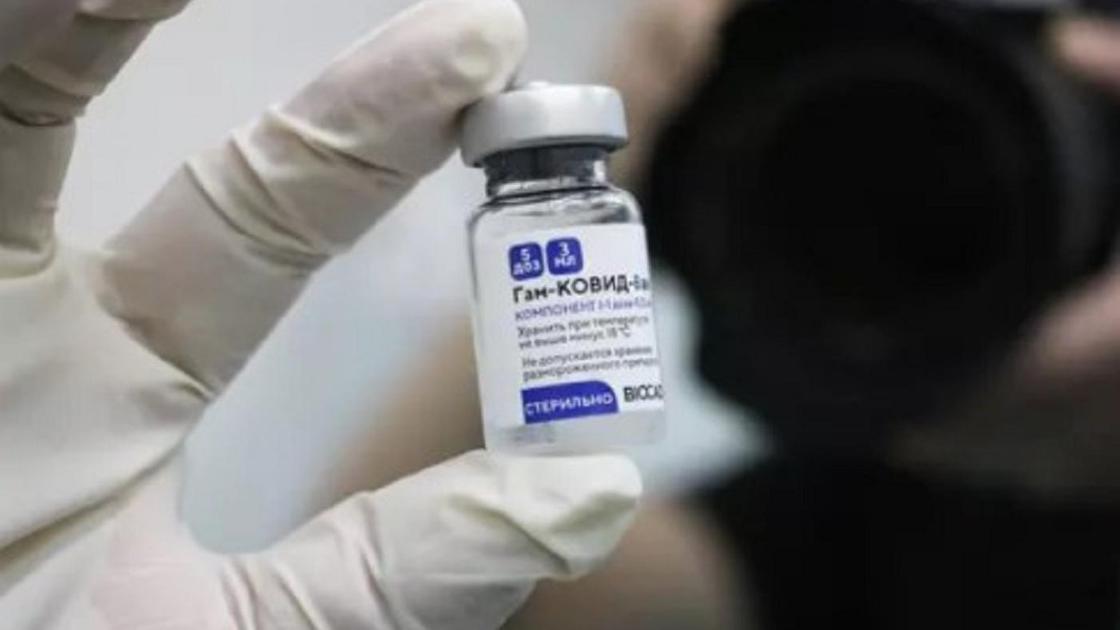
1 ақпанда Қазақстанда коронавирусқа қарсы жаппай вакцинация басталды. Азаматтарға ресейлік "Спутник V" препараты егілуде. KAZ.NUR.KZ журналистері ақпаратпен танысу үшін дәрігерлерден препараттың толық аннотациясын көрсетуін өтінді.
"Шайқамау": вакцинаның нақты атауы және сақтау талаптары
Вакцинаның қаптамасында "Гам-КОВИД-Вак" - Sars-CoV-2 вирусынан туындаған (Covid-19 жаңа коронавирус инфекциясынан) коронавирустық инфекцияның алдын алуға арналған аралас векторлы вакцина деп жазылған.
Біз қаптама мен вакцинаның бірінші бөлігі - 1 компонент флаконды фотоға түсірдік. 2 компонент пациентке 21 күннен кейін енгізіледі.
Иықтың жоғарғы үштен біріндегі бұлшықет ішіне немесе жамбастың латералды бұлшықетіне енгізіледі. Тамырға салуға тыйым салынған.

Біздің көзімізше флакон тоңазытқыштан алынды. Ол мұз болып қатып қалған. Дәрігер оның бөлме температурасында толық ерігенінше күтуі керек.
Қалған мұз қоспаларына жол берілмейді, флаконды шайқауға тыйым салынады. Ішіндегісін тек сілку арқылы араластыруға болады.
Сақтау температурасы -18 градустан аспауы тиіс.
Өндіруші: Ресей, Владимирский облысы, "ГЕНЕРИУМ"АҚ.
2 сағатта 5 адамға екпе салу
Флаконда 3 мл сұйық зат бар - бұл 0,5 мл-ден 5 доза.
Ерітілгеннен кейін флаконды 2 сағаттан артық сақтауға болмайды. Қайтадан ерітуге тыйым салынған. Бұл дәрігер 2 сағаттың ішінде 5 адамға екпе салуы керектігін білдіреді немесе препараттың қалдығын жою керек.
Вакцина құрамы - 1-компонент және 2-компонент
1-компоненттің құрамы: 26 серотипті адам аденовирусына негізделген рекомбинантты аденовирустық вектор, SARS-CoV-2 вирусының S ақуызы генін тасушы.
2-компоненттің құрамы: 5 серотипті адам аденовирусына негізделген рекомбинантты аденовирус векторы, SARS-CoV-2 вирусының S ақуызы генін тасушы.
Екі компоненттегі қосымша заттар: трис (гидроксиметил), аминометан, натрий хлорид, сахароза, полисорбат 80, гексагидрат магний хлориді, этилендиаминтетра сірке қышқылының динатрий тұзы, этанол 95%, инъекцияға арналған су.

Вакцина нұсқаулығындағы алғашқы жолдарда
"Бұл препарат төтенше жағдайлардың пайда болу және жою қаупі жағдайында қолдану үшін препараттарды тіркеу процедурасы бойынша тіркелген.
Нұсқаулық шектеулі клиникалық мәліметтер негізінде дайындалған және жаңа деректер пайда болған кезде жаңартылады" деп жазылған.
Қарсы көрсетілімдер
- ұқсас компоненттері бар вакцинаның немесе вакцинаның кез-келген компонентіне жоғары сезімталдық,
- сыртартқыдағы ауыр аллергиялық реакциялар,
- жедел жұқпалы және инфекциялық емес аурулар, созылмалы аурулардың өршуі - вакцинация қалпына келтіруден немесе ремиссиядан кейін 2-4 аптадан кейін жүргізіледі. Жеңіл ЖРВИ, асқазан-ішек жолдарының жедел жұқпалы аурулары кезінде температура қалыпқа келгеннен кейін вакцинация жасалады.
- жүктілік және бала емізу кезеңі,
- 18 жасқа дейін (тиімділігі мен қауіпсіздігі туралы деректердің болмауына байланысты).
2 компонентті енгізуге қарсы көрсетілімдер: 1-компонентті енгізу кезіндегі вакцинадан кейінгі ауыр асқынулар (анафилактикалық шок, ауыр жайылған аллергиялық реакциялар, ұстама синдромы, 40 градустық температура және т.б.).
Препаратты келесі жағдайларда сақтықпен қолданыңыз:
- бауыр мен бүйректің созылмалы аурулары,
- эндокриндік аурулар (декомпенсация сатысында қалқанша безінің және қант диабеті қызметінің бұзылуы),
- қан түзуші жүйенің ауыр аурулары,
- эпилепсия және басқа да орталық жүйке аурулары,
- жедел коронарлық синдром және ми қан айналымының жедел бұзылуы,
- миокардит, эндокардит, перикардит.
Ақпараттың жеткілікті болмауына байланысты вакцинация келесі топтағы адамдарға қауіп төндіруі мүмкін:
- аутоиммунды аурулармен (иммундық жүйені ынталандыру аурудың өршуіне әкелуі мүмкін, әсіресе ауыр және өмірге қауіп төндіретін жағдайларды жасауға бейім аутоиммундық патологиясы бар науқастарға сақтықпен қарау керек)
- жаңадан пайда болған қатерлі ісіктер.
Вакцинация туралы шешім әр нақты жағдайда пайда мен тәуекел балансын бағалауға негізделуі керек.
Басқа препараттармен өзара әрекеттесуі - зерттеу жүргізілмеген.
Көлік құралын басқаруға әсер ету ерекшеліктері - зерттеулер жүргізілген жоқ.
Вакцинаның жағымсыз реакциялары
Жағымсыз реакциялар вакцинациядан кейінгі бірінші немесе екінші күні дамуы мүмкін және кейінгі 3 күн ішінде жойылады.
Жиі: бас ауруы, әлсіздену, астения, миалгия, артралгия, дене температурасының көтерілуі секілді қысқа мерзімді тұмауға ұқсас синдром.
Сондай-ақ жұтқыншақтағы ауырсыну, мұрын бітелуі, тамақ ауруы, ринорея, жүрек айну, құсу, тәбеттің төмендеуі, диспепсия.
Гиперемиямен, ісінумен, қышумен инъекция орнында ауру түріндегі жергілікті реакциялар.
Кейде: аймақтық лимфа түйіндерінің ұлғаюы, кейбіреулерінде аллергия болуы мүмкін, бауыр трансаминазалары, креатинин және қан сарысуындағы креатинфосфокиназа деңгейінің қысқа мерзімді жоғарылауы.
Сирек: бас айналу мен естен тану.

Қарағанды фармацевтикалық кешені - дәрілік заттардың сапасына шағымдарды қабылдайтын, сондай-ақ Қазақстандағы вакциналардың қауіпсіздігін қадағалауға жауапты ұйым.
Мақаланың түпнұсқасы: https://kaz.nur.kz/society/1897129-kazakstandyktarga-salynyp-zatkan-sputnik-v-vakcinasyny-nskaulygynda-ne-zazylgan/
